Степени окисления меди возможные – Степень окисления меди (Cu), формула и примеры
alexxlab | 14.07.2020 | 0 | Разное
Химический состав
Химические свойства
Возможные степени окисления
В соединениях медь проявляет две степени окисления: +1 и +2. Первая из них склонна к диспропорционированию и устойчива только в нерастворимых соединениях (Cu2O, CuCl, CuI и т. п.) или комплексах (например, [Cu(Nh4)2]+). Её соединения бесцветны. Более устойчива степень окисления +2, которая даёт соли синего и сине-зелёного цвета. В необычных условиях можно получить соединения со степенью окисления +3 и даже +5. Последняя встречается в солях купраборанового аниона Cu(B11h21)23−, полученных в 1994 году.
Не изменяется на воздухе в отсутствие влаги и диоксида углерода. Является слабым восстановителем, не вступает в реакцию с водой и разбавленной соляной кислотой. Переводится враствор кислотами-неокислителями или гидратом аммиака в присутствии кислорода, цианидом калия. Окисляется концентрированными серной и азотной кислотами, «царской водкой», кислородом, галогенами, халькогенами, оксидами неметаллов. Вступает в реакцию при нагревании с галогеноводородами.
На влажном воздухе медь окисляется, образуя основный карбонат меди(II) (внешний слой патины):
На влажном воздухе медь окисляется, образуя основный карбонат меди(II) (внешний слой патины):
2Cu + h3O + CO2 + O2 à Cu2CO3(OH)2↓
Реагирует с концентрированной холодной серной кислотой:
Cu + h3SO1 àCuO + SO2 ↑ + h3O
С концентрированной горячей серной кислотой:
Cu + 2h3SO4 à CuSO4 + SO2 ↑ + 2h3O
- В электротехнике
- Теплообмен
- Для производства труб
- Сплавы
- Сплавы на основе меди
- Сплавы, в которых медь значима
- Ювелирные сплавы
- Соединения меди
Из-за низкого удельного сопротивления (уступает лишь серебру, удельное сопротивление при 20 °C: 0,01724-0,0180 мкОм·м), медь широко применяется в электротехнике для изготовления силовых и других кабелей, проводов или других проводников, например, при печатном монтаже. Медные провода, в свою очередь, также используются в обмотках электроприводов (быт: электродвигателях) и силовых трансформаторов. Для этих целей металл должен быть очень чистый: примеси резко снижают электрическую проводимость. Например, присутствие в меди 0,02 % алюминия снижает её электрическую проводимость почти на 10 %.
Другое полезное качество меди — высокая теплопроводность. Это позволяет применять её в различных теплоотводных устройствах, теплообменниках, к числу которых относятся и широко известныерадиаторы охлаждения, кондиционирования и отопления, компьютерных кулерах, тепловых трубках.
В связи с высокой механической прочностью и пригодностью для механической обработки медные бесшовные трубы круглого сечения получили широкое применение для транспортировки жидкостей и газов: во внутренних системах водоснабжения, отопления, газоснабжения, системах кондиционирования и холодильных агрегатах. В ряде стран трубы из меди являются основным материалом, применяемым для этих целей: во Франции, Великобритании и Австралии для газоснабжения зданий, в Великобритании, США, Швеции и Гонконге для водоснабжения, в Великобритании и Швеции для отопления.
В России производство водогазопроводных труб из меди нормируется национальным стандартом ГОСТ Р 52318-2005, а применение в этом качестве федеральным Сводом Правил СП 40-108-2004. Кроме того, трубопроводы из меди и сплавов меди широко используются в судостроении и энергетике для транспортировки жидкостей и пара.
В разнообразных областях техники широко используются сплавы с использованием меди, самыми широко распространёнными из которых являются упоминавшиеся выше бронза и латунь. Оба сплава являются общими названиями для целого семейства материалов, в которые, помимо олова и цинка, могут входить никель, висмут и другие металлы. Например, в состав пушечной бронзы, использовавшейся для изготовления артиллерийских орудий вплоть до XIX века, входят все три основных металла — медь, олово, цинк; рецептура менялась от времени и места изготовления орудия. Большое количество латуни идёт на изготовление гильз артиллерийских боеприпасов и оружейных гильз, благодаря технологичности и высокой пластичности. Для деталей машин используют сплавы меди с цинком, оловом, алюминием, кремнием и др. (а не чистую медь) из-за их большей прочности: 30—40 кгс/мм² у сплавов и 25—29 кгс/мм² у технически чистой меди. Медные сплавы (кроме бериллиевой бронзы и некоторых алюминиевых бронз) не изменяют механических свойств при термической обработке, и их механические свойства и износостойкость определяются только химическим составом и его влиянием на структуру. Модуль упругости медных сплавов (900—12000 кгс/мм², ниже, чем у стали). Основное преимущество медных сплавов — низкий коэффициент трения (что делает особенно рациональным применением их в парах скольжения), сочетающийся для многих сплавов с высокой пластичностью и хорошей стойкостью против коррозии в ряде агрессивных сред (медно-никелевые сплавы и алюминиевые бронзы) и хорошей электропроводностью. Величина коэффициента трения практически одинакова у всех медных сплавов, тогда как механические свойства и износостойкость, а также поведение в условиях коррозии зависят от состава сплавов, а следовательно, от структуры. Прочность выше у двухфазных сплавов, а пластичность у однофазных. Медноникелевый сплав (мельхиор) используются для чеканки разменной монеты. Медноникелевые сплавы, в том числе и так называемый «адмиралтейский» сплав, широко используются в судостроении (трубки конденсаторов отработавшего пара турбин, охлаждаемых забортной водой) и областях применения, связанных с возможностью агрессивного воздействия морской воды из-за высокой коррозионной устойчивости. Медь является важным компонентом твёрдых припоев — сплавов с температурой плавления 590—880 градусов Цельсия, обладающих хорошей адгезией к большинству металлов, и применяющихся для прочного соединения разнообразных металлических деталей, особенно из разнородных металлов, от трубопроводной арматуры до жидкостных ракетных двигателей.
Дюраль (дюралюминий) определяют как сплав алюминия и меди (меди в дюрали 4,4 %).
В ювелирном деле часто используются сплавы меди с золотом для увеличения прочности изделий к деформациям и истиранию, так как чистое золото — очень мягкий металл и нестойко к механическим воздействиям.
Оксиды меди используются для получения оксида иттрия бария меди YBa2Cu3O7-δ, который является основой для получения высокотемпературных сверхпроводников. Медь применяется для производства медно-окисных гальванических элементов и батарей.
metromet.ru
Химические свойства
Возможные степени окисления
В соединениях медь проявляет две степени окисления: +1 и +2. Первая из них склонна к диспропорционированию и устойчива только в нерастворимых соединениях (Cu2O, CuCl, CuI и т. п.) или комплексах (например [Cu(NH3)2]+. Её соединения бесцветны. Более устойчива степень окисления +2, которая даёт соли синего и сине-зелёного цвета. В необычных условиях можно получить соединения со степенью окисления +3 и даже +5. Последняя встречается в солях купраборанового аниона Cu(B11H11)23−, полученных в 1994 году.
Не изменяется на воздухе в отсутствие влаги и диоксида углерода. Является слабым восстановителем, не реагирует с водой, разбавленнойсоляной кислотой. Переводится в раствор кислотами-неокислителями или гидратом аммиака в присутствии кислорода, цианидом калия. Окисляется концентрированными серной и азотной кислотами, «царской водкой», кислородом, галогенами, халькогенами, оксидаминеметаллов. Реагирует при нагревании с галогеноводородами.
На влажном воздухе медь окисляется, образуя основный карбонат меди(II):
Реагирует с концентрированной холодной серной кислотой:
С концентрированной горячей серной кислотой:
С безводной серной кислотой при 200 °C:
C разбавленной серной кислотой при нагревании в присутствии кислорода воздуха:
Реагирует с концентрированной азотной кислотой:
С разбавленной азотной кислотой:
С царской водкой:
С концентрированной горячей соляной кислотой:
C разбавленной хлороводородной кислотой в присутствии кислорода:
С газообразным хлороводородом при 500—600 °C:
С бромоводородом:
Также медь реагирует с концентрированной уксусной кислотой в присутствии кислорода:
Медь растворяется в концентрированном гидроксиде аммония, с образованием аммиакатов:
Окисляется до оксида меди(I) при недостатке кислорода и 200 °C и до оксида меди(II), при избытке кислорода и температурах порядка 400—500 °C:
Медный порошок реагирует с хлором, серой (в жидком сероуглероде) и бромом (в эфире), при комнатной температуре:
При 300—400 °C реагирует с серой и селеном:
C оксидами неметаллов:
Медь реагирует с цианидом калия с образованием дицианокупрата(I) калия, щелочи и водорода:
С концентрированной соляной кислотой и хлоратом калия:
Соединения меди(I)
Степени окисления +1 соответствует оксид Cu2O красно-оранжевого цвета. Соответствующий гидроксид CuOH (жёлтого цвета) быстро разлагается с образованием оксида. Гидроксид CuOH проявляет основные свойства.
Многие соединения меди +1 имеют белую окраску либо бесцветны. Это объясняется тем, что в ионе Сu+ все пять Зd-оны меди(I) в водном растворе неустойчивы и легко диспропорционируют:
Серебро́ — элемент 11 группы (по устаревшей классификации — побочной подгруппы первой группы), пятого периодапериодической системы химических элементов Д. И. Менделеева, с атомным номером 47. Обозначается символом Ag(лат. Argentum).
Простое вещество серебро (CAS-номер: 7440-22-4) — ковкий, пластичный благородный металл серебристо-белого цвета.Кристаллическая решётка — гранецентрированная кубическая. Температура плавления — 962 °C, плотность — 10,5 г/см³.
Похожие статьи:
poznayka.org
Валентность меди (Cu), формулы и примеры
Общие сведения о валентности меди
Медь представляет собой металл красного цвета с гранецентрированной кубической решеткой. Медь характеризуется исключительной пластичностью и превосходит другие металлы по теплопроводности и электрической проводимости. Плотность 8,94 г/см3. Температура плавления 1084,5oС, кипения 2540oС.
Валентность меди в соединениях
Медь – двадцать девятый по счету элемент Периодической таблицы Д.И. Менделеева. Он находится в четвертом периоде в IВ группе. В ядре атома меди содержится 29 протонов и 35 нейтронов (массовое число равно 64). В атоме меди есть четыре энергетических уровня, на которых находятся 29 электронов (рис. 1).
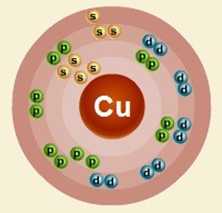
Рис. 1. Строение атома меди.
Электронная формула атома меди в основном состоянии имеет следующий вид:
1s22s22p63s23p63d104s1.
А энергетическая диаграмма (строится только для электронов внешнего энергетического уровня, которые по-другому называют валентными):
Наличие одного неспаренного электрона свидетельствует о том, что медь проявляет в своих соединениях валентность I (Cu2O, CuOH).Известно, что для меди также характерна валентность II (CuO, Cu(OH)2, CuSO4).
Примеры решения задач
| Понравился сайт? Расскажи друзьям! | |||
ru.solverbook.com
Возможные степени окисления
В соединениях медь проявляет две степени окисления: +1 и +2. Первая из них склонна к диспропорционированию и устойчива только в нерастворимых соединениях (Cu2O, CuCl, CuI и т. п.) или комплексах (например, [Cu(NH3)2]+). Её соединения бесцветны. Более устойчива степень окисления +2, которая даёт соли синего и сине-зелёного цвета. В необычных условиях можно получить соединения со степенью окисления +3 и даже +5. Последняя встречается в солях купраборанового аниона Cu(B11H11)23−, полученных в 1994 году.
Простое вещество[править | править вики-текст]
Не изменяется на воздухе в отсутствие влаги и диоксида углерода. Является слабым восстановителем, не вступает в реакцию с водой и разбавленной соляной кислотой. Переводится в раствор кислотами-неокислителями или гидратом аммиака в присутствии кислорода, цианидом калия. Окисляется концентрированными серной и азотной кислотами, «царской водкой», кислородом, галогенами, халькогенами, оксидами неметаллов. Вступает в реакцию при нагревании с галогеноводородами.
На влажном воздухе медь окисляется, образуя основный карбонат меди(II) (внешний слой патины):
Реагирует с концентрированной холодной серной кислотой:
С концентрированной горячей серной кислотой:
С безводной горячей серной кислотой:
C разбавленной серной кислотой при нагревании в присутствии кислорода воздуха:
С концентрированной азотной кислотой:
С разбавленной азотной кислотой:
С “царской водкой”:
С концентрированной горячей соляной кислотой:
C разбавленной хлороводородной кислотой в присутствии кислорода:
С газообразным хлороводородом при 500—600 °C:
С бромоводородом:
Также медь реагирует с концентрированной уксусной кислотой в присутствии кислорода:
Медь растворяется в концентрированном гидроксиде аммония, с образованием аммиакатов:
Окисляется до оксида меди(I) при недостатке кислорода и 200 °C и до оксида меди(II), при избытке кислорода и температурах порядка 400—500 °C:
Медный порошок реагирует с хлором, серой (в жидком сероуглероде) и бромом (в эфире), при комнатной температуре:
При 300—400 °C реагирует с серой и селеном:
C оксидами неметаллов:
Медь реагирует с цианидом калия с образованием дицианокупрата(I) калия, щелочи и водорода:
С концентрированной соляной кислотой и хлоратом калия:
Соединения меди(I)[править | править вики-текст]
Степени окисления +1 соответствует оксид Cu2O красно-оранжевого цвета. Соответствующий гидроксид CuOH (жёлтого цвета) быстро разлагается с образованием оксида. Гидроксид CuOH проявляет основные свойства.
Многие соединения меди +1 имеют белую окраску либо бесцветны. Это объясняется тем, что в ионе Сu+ все пять Зd-орбиталей заполнены парами электронов.
Ионы меди(I) в водном растворе неустойчивы и легко диспропорционируют:
В то же время медь(I) встречается в форме соединений, которые не растворяются в воде, либо в составе комплексов. Например, дихлорокупрат(I)-ион [CuCl2]− устойчив. Его можно получить, добавляя концентрированную соляную кислоту к хлориду меди(I):
Свойства соединений меди (I) похожи на свойства соединений серебра (I). В частности, CuCl, CuBr и CuI нерастворимы. Также существует нестабильный сульфат меди(I).
Соединения меди(II)[править | править вики-текст]
Степень окисления II — наиболее стабильная степень окисления меди. Ей соответствует чёрный оксид CuO и голубой гидроксид Cu(OH)2, который при стоянии легко отщепляет воду и при этом чернеет:
Гидроксид меди (II) носит преимущественно основный характер и только в концентрированной щелочи частично растворяется с образованием синего гидроксокомплекса. Наибольшее значение имеет реакция гидроксида меди (II) с водным раствором аммиака, при которой образуется так называемый реактив Швейцера (растворитель целлюлозы):
Соли меди(II) образуются при растворении меди в кислотах-окислителях (азотной, концентрированной серной). Большинство солей в этой степени окисления имеют синюю или зелёную окраску.
Соединения меди(II) обладают слабыми окислительными свойствами, что используется в анализе (например, использование реактива Фелинга).
Карбонат меди(II) имеет зелёную окраску, что является причиной позеленения элементов зданий, памятников и изделий из меди и медных сплавов при взаимодействии оксидной плёнки с углекислым газом воздуха в присутствии воды. Сульфат меди(II) при гидратации даёт синие кристаллы медного купороса CuSO4∙5H2O, используется как фунгицид.
Оксид меди (II) используются для получения оксида иттрия бария меди (YBa2Cu3O7-δ), который является основой для получения сверхпроводников.
Соединения меди(III) и меди(IV)[править | править вики-текст]
Степени окисления III и IV являются малоустойчивыми степенями окисления и представлены только соединениями с кислородом, фтором или в виде комплексов.
3-net.ru
|
Порядковый номер |
Русское / англ. название |
Химический символ |
Степень окисления |
|
1 |
Водород / Hydrogen |
H |
(+1), (-1) |
|
2 |
Гелий / Helium |
He |
0 |
|
3 |
Литий / Lithium |
Li |
(+1) |
|
4 |
Бериллий / Beryllium |
Be |
(+2) |
|
5 |
Бор / Boron |
B |
(-1), 0, (+1), (+2), (+3) |
|
6 |
Углерод / Carbon |
C |
(-4), (-3), (-2), (-1), 0, (+2), (+4) |
|
7 |
Азот / Nitrogen |
N |
(-3), (-2), (-1), 0, (+1), (+2), (+3), (+4), (+5) |
|
8 |
Кислород / Oxygen |
O |
(-2), (-1), 0, (+1), (+2) |
|
9 |
Фтор / Fluorine |
F |
(-1) |
|
10 |
Неон / Neon |
Ne |
0 |
|
11 |
Натрий / Sodium |
Na |
(+1) |
|
12 |
Магний / Magnesium |
Mg |
(+2) |
|
13 |
Алюминий / Aluminum |
Al |
(+3) |
|
14 |
Кремний / Silicon |
Si |
(-4), 0, (+2), (+4) |
|
15 |
Фосфор / Phosphorus |
P |
(-3), 0, (+3), (+5) |
|
16 |
Сера / Sulfur |
S |
(-2), 0, (+4), (+6) |
|
17 |
Хлор / Chlorine |
Cl |
(-1), 0, (+1), (+3), (+5), (+7), редко (+2) и (+4) |
|
18 |
Аргон / Argon |
Ar |
0 |
|
19 |
Калий / Potassium |
K |
(+1) |
|
20 |
Кальций / Calcium |
Ca |
(+2) |
|
21 |
Скандий / Scandium |
Sc |
(+3) |
|
22 |
Титан / Titanium |
Ti |
(+2), (+3), (+4) |
|
23 |
Ванадий / Vanadium |
V |
(+2), (+3), (+4), (+5) |
|
24 |
Хром / Chromium |
Cr |
(+2), (+3), (+6) |
|
25 |
Марганец / Manganese |
Mn |
(+2), (+3), (+4), (+6), (+7) |
|
26 |
Железо / Iron |
Fe |
(+2), (+3), редко (+4) и (+6) |
|
27 |
Кобальт / Cobalt |
Co |
(+2), (+3), редко (+4) |
|
28 |
Никель / Nickel |
Ni |
(+2), редко (+1), (+3) и (+4) |
|
29 |
Медь / Copper |
Cu |
+1, +2, редко (+3) |
|
30 |
Цинк / Zinc |
Zn |
(+2) |
|
31 |
Галлий / Gallium |
Ga |
(+3), редко (+2) |
|
32 |
Германий / Germanium |
Ge |
(-4), (+2), (+4) |
|
33 |
Мышьяк / Arsenic |
As |
(-3), (+3), (+5), редко (+2) |
|
34 |
Селен / Selenium |
Se |
(-2), (+4), (+6), редко (+2) |
|
35 |
Бром / Bromine |
Br |
(-1), (+1), (+5), редко (+3), (+4) |
|
36 |
Криптон / Krypton |
Kr |
0 |
|
37 |
Рубидий / Rubidium |
Rb |
(+1) |
|
38 |
Стронций / Strontium |
Sr |
(+2) |
|
39 |
Иттрий / Yttrium |
Y |
(+3) |
|
40 |
Цирконий / Zirconium |
Zr |
(+4), редко (+2) и (+3) |
|
41 |
Ниобий / Niobium |
Nb |
(+3), (+5), редко (+2) и (+4) |
|
42 |
Молибден / Molybdenum |
Mo |
(+3), (+6), редко (+2), (+3) и (+5) |
|
43 |
Технеций / Technetium |
Tc |
(+6) |
|
44 |
Рутений / Ruthenium |
Ru |
(+3), (+4), (+8), редко (+2), (+6) и (+7) |
|
45 |
Родий / Rhodium |
Rh |
(+4), редко (+2), (+3) и (+6) |
|
46 |
Палладий / Palladium |
Pd |
(+2), (+4), редко (+6) |
|
47 |
Серебро / Silver |
Ag |
(+1), редко (+2) и (+3) |
|
48 |
Кадмий / Cadmium |
Cd |
(+2), редко (+1) |
|
49 |
Индий / Indium |
In |
(+3), редко (+1) и (+2) |
|
50 |
Олово / Tin |
Sn |
(+2), (+4) |
|
51 |
Сурьма / Antimony |
Sb |
(-3), (+3), (+5), редко (+4) |
|
52 |
Теллур / Tellurium |
Te |
(-2), (+4), (+6), редко (+2) |
|
53 |
Иод / Iodine |
I |
(-1), (+1), (+5), (+7), редко (+3), (+4) |
|
54 |
Ксенон / Xenon |
Xe |
0 |
|
55 |
Цезий / Cesium |
Cs |
(+1) |
|
56 |
Барий / Barium |
BA |
(+2) |
|
57 |
Лантан / Lanthanum |
La |
(+3) |
|
58 |
Церий / Cerium |
Ce |
(+3), (+4) |
|
59 |
Празеодим / Praseodymium |
Pr |
(+3) |
|
60 |
Неодим / Neodymium |
Nd |
(+3), (+4) |
|
61 |
Прометий / Promethium |
Pm |
(+3) |
|
62 |
Самарий / Samarium |
Sm |
(+3), редко (+2) |
|
63 |
Европий / Europium |
Eu |
(+3), редко (+2) |
|
64 |
Гадолиний / Gadolinium |
Gd |
(+3) |
|
65 |
Тербий / Terbium |
Tb |
(+3), (+4) |
|
66 |
Диспрозий / Dysprosium |
Dy |
(+3) |
|
67 |
Гольмий / Holmium |
Ho |
(+3) |
|
68 |
Эрбий / Erbium |
Er |
(+3) |
|
69 |
Тулий / Thulium |
Tm |
(+3), редко (+2) |
|
70 |
Иттербий / Ytterbium |
Ib |
(+3), редко (+2) |
|
71 |
Лютеций / Lutetium |
Lu |
(+3) |
|
72 |
Гафний / Hafnium |
Hf |
(+4) |
|
73 |
Тантал / Tantalum |
Ta |
(+5), редко (+3), (+4) |
|
74 |
Вольфрам / Tungsten |
W |
(+6), редко (+2), (+3), (+4) и (+5) |
|
75 |
Рений / Rhenium |
Re |
(+2), (+4), (+6), (+7), редко (-1), (+1), (+3), (+5) |
|
76 |
Осмий / Osmium |
Os |
(+3), (+4), (+6), (+8), редко (+2) |
|
77 |
Иридий / Iridium |
Ir |
(+3), (+4), (+6), редко (+1) и (+2) |
|
78 |
Платина / Platinum |
Pt |
(+2), (+4), (+6), редко (+1) и (+3) |
|
79 |
Золото / Gold |
Au |
(+1), (+3), редко (+2) |
|
80 |
Ртуть / Mercury |
Hg |
(+1), (+2) |
|
81 |
Талий / Thallium |
Tl |
(+1), (+3), редко (+2) |
|
82 |
Свинец / Lead |
Pb |
(+2), (+4) |
|
83 |
Висмут / Bismuth |
Bi |
(+3), редко (+3), (+2), (+4) и (+5) |
|
84 |
Полоний / Polonium |
Po |
(+2), (+4), редко (-2) и (+6) |
|
85 |
Астат / Astatine |
At |
— |
|
86 |
Радон / Radon |
Ra |
0 |
|
87 |
Франций / Francium |
Fr |
— |
|
88 |
Радий / Radium |
Ra |
(+2) |
|
89 |
Актиний / Actinium |
Ac |
(+3) |
|
90 |
Торий / Thorium |
Th |
(+4) |
|
91 |
Проактиний / Protactinium |
Pa |
(+5) |
|
92 |
Уран / Uranium |
U |
(+3), (+4), (+6), редко (+2) и (+5) |
ru.solverbook.com
Степень – окисление – медь
Степень – окисление – медь
Cтраница 1
Степень окисления меди в церулоплазмине первоначально была определена химическими методами с помощью избирательных реагентов на ионы меди ( II) [38], а позже – методами полярографии и ЭПР. Ионы меди ( 1) церулоплазмина окисляются только при разрушении белка, хотя ионы Си ( II) могут восстанавливаться обратимо. [2]
Определение степени окисления меди с помощью рентгеног электронной спектроскопии облегчается тем, что линии Си2р в спектре соединений Си11 сопровождаются интенсивными сателлитами, в спектрах диамагнитных соединений Си1 они отсутствуют. [3]
Как изменяется степень окисления меди в этой реакции. [4]
Это соединение является интересным примером стабилизации двух степеней окисления меди за счет комплексообразования. Синтез его включает несколько стадий. [5]
В этом комплексе возможен перенос протона аминогруппы органической части молекулы к атому кислорода или перенос электрона без формального изменения степени окисления меди. [6]
Какие степени окисления меди известны. [7]
Какие степени окисления проявляет медь в своих соединениях. Соединения с какой степенью окисления меди наиболее устойчивы. [8]
Окисномедный электрод получается при анодной поляризации меди в щелочном растворе. При 0 7 В степень окисления меди повышается и образуется GuO, а при более высоком потенциале начинается выделение кислорода. Если концентрация щелочи недостаточно – велика, может начаться растворение меди. [9]
Окисномедный электрод получается при анодной поляризации меди в щелочном растворе. При 0 7 В степень окисления меди повышается и образуется СиО, а при более высоком потенциале начинается выделение кислорода. Если концентрация щелочи недостаточно велика, может начаться растворение меди. [10]
Окисномедный электрод получается при анодной поляризации меди в щелочном растворе. При 0 7 В степень окисления меди повышается и образуется СпО, а при более высоком потенциале начинается выделение кислорода. Если концентрация щелочи недостаточно велика, может начаться растворение меди. [11]
Страницы: 1
www.ngpedia.ru

