Физические свойства углекислого газа – Физические и химические свойства углекислого газа
alexxlab | 31.01.2019 | 0 | Вопросы и ответы
|
Физические свойства углекислоты Углекислота (СО2, двуокись углерода, диоксид углерода) – вещество с химическое формулой СО2 и молекулярной массой 44,011 г/моль, которое может существовать в четырёх фазовых состояниях – газообразном, жидком, твёрдом и сверхкритическом. Газообразное состояние СО2 носит общеупотребительное название «углекислый газ». При атмосферном давлении это бесцветный газ без цвета и запаха, при температуре +20 ?С плотностью 1,839 кг/м? (в 1,52 раза тяжелее воздуха), хорошо растворяется в воде (0,88 объёма в 1 объёме воды), частично взаимодействуя в ней с образованием угольной кислоты. Входит в состав атмосферы в среднем 0,035% по объёму. При резком охлаждении за счёт расширения (детандирование) СО2 способен десублимироваться – переходить сразу в твёрдое состояние, минуя жидкую фазу. Газообразный диоксид углерода ранее нередко хранили в стационарных газгольдерах. В настоящее время такой способ хранения не применяется; углекислый газ в необходимом количестве получают непосредственно на месте – путём испарения жидкой углекислоты в газификаторе. Далее газ можно легко перекачать по любому газопроводу под давлением 2-6 атмосфер. Жидкое состояние СО2 носит техническое название «жидкая углекислота» или просто «углекислота». Это бесцветная жидкость без запаха, средней плотностью 771 кг/м3, которая существует только под давлением 3 482…519 кПа при температуре 0…-56,5 град.С («низкотемпературная углекислота»), либо под давлением 3 482…7 383 кПа при температуре 0…+31,0 град.С («углекислота высокого давления»). Углекислоту высокого давления получают чаще всего путём сжатия углекислого газа до давления конденсации, при одновременном охлаждении водой. Низкотемпературную углекислоту, являющейся основной формой диоксида углерода для промышленного потребления, чаще всего получают по циклу высокого давления путём трехступенчатого охлаждения и дросселирования в специальных установках. При небольшом и среднем потреблении углекислоты (высокого давления),т для её хранения и транспортировки используют разнообразные стальные баллоны (от баллончиков для бытовых сифонов до ёмкостей вместимостью 55 л). Самым распространенным является 40 л баллон с рабочим давление 15 000 кПа, вмещающим 24 кг углекислоты. За стальными баллонами не требуется дополнительный уход, углекислота сохраняется без потерь в течение длительного времени. Баллоны с углекислотой высокого давления окрашивают в чёрный цвет. При значительном потреблении, для хранения и транспортировки низкотемпературной жидкой углекислоты используют изотермические цистерны самой разнообразной вместимости, оснащённые служебными холодильными установками. Существуют накопительные (стационарные) вертикальные и горизонтальные цистерны вместимостью от 3 до 250 т, транспортируемые цистерны вместимостью от 3 до 18 т. Цистерны вертикального исполнения требуют строительства фундамента и используются преимущественно в условиях ограниченного пространства для размещения. Применение горизонтальных цистерн позволяет снизить затраты на фундаменты, особенно при наличии общей рамы с углекислотной станцией. Цистерны состоят из внутреннего сварного сосуда, изготовленного из низкотемпературной стали и имеющего пенополиуретановую или вакуумную теплоизоляцию; наружного кожуха из пластика, оцинкованной или нержавеющей стали; трубопроводов, арматуры и приборов контроля. Внутренняя и наружная поверхности сварного сосуда подвергаются специальной обработке, благодаря чему снижена до вероятность поверхностной коррозии металла. В дорогих импортных моделях наружный герметичный кожух выполнен из алюминия. Использование цистерн обеспечивает заправку и слив жидкой углекислоты; хранение и транспортировку без потерь продукта; визуальный контроль массы и рабочего давления при заправке, в процессе хранения и выдачи. Все типы цистерн оснащены многоуровневой системой безопасности. Предохранительные клапаны позволяют производить проверку и ремонт без остановки и опорожнения цистерны. При мгновенном снижении давления до атмосферного, происходящем при впрыске в специальную расширительную камеру (дросселировании), жидкий диоксид углерода мгновенно превращается в газ и тончайшую снегообразную массу, которую прессуют и получают диоксид углерода в твёрдом состоянии, который носит общеупотребительное название «сухой лёд». При атмосферном давлении это белая стекловидная масса плотностью 1 562 кг/м?, с температурой -78,5 ?С, которая на открытом воздухе сублимируется – постепенно испаряется, минуя жидкое состояние. Сухой лёд может быть также получен непосредственно на установках высокого давления, применяемых для получения низкотемпературной углекислоты, из газовых смесей, содержащих СО2 в количестве не менее 75-80%. Объёмная холодопроизводительность сухого льда почти в 3 раза больше, чем у водяного льда, и составляет 573,6 кДж/кг. Твёрдый диоксид углерода обычно выпускают в брикетах размером 200?100?20-70 мм, в гранулах диаметром 3, 6, 10, 12 и 16 мм, редко в виде тончайшего порошка («сухой снег»). Брикеты, гранулы и снег хранят не более 1-2 суток в стационарных заглублённых хранилищах шахтного типа, разбитых на небольшие отсеки; перевозят в специальных изотермических контейнерах с предохранительным клапаном. Используются контейнеры разных производителей вместимостью от 40 до 300 кг и более. Потери на сублимацию составляют, в зависимости от температуры окружающего воздуха 4-6% и более в сутки. При давлении свыше 7,39 кПа и температуре более 31,6 град.С диоксид углерода находится в так называемом сверхкритическом состоянии, при котором его плотность как у жидкости, а вязкость и поверхностное натяжение как у газа. Эта необычная физическая субстанция (флюид) является отличным неполярным растворителем. Сверхкритический CO2 способен полностью или выборочно экстрагировать любые неполярные составляющие с молекулярной массой менее 2 000 дальтон: терпеновые соединения, воски, пигменты, высокомолекулярные насыщенные и ненасыщенные жирные кислоты, алкалоиды, жирорастворимые витамины и фитостерины. Нерастворимыми веществами для сверхкритического CO2 являются целлюлоза, крахмал, органические и неорганические полимеры с высоким молекулярным весом, сахара, гликозидные вещества, протеины, металлы и соли многих металлов. Обладая подобными свойствами, сверхкритический диоксид углерода всё шире применяется в процессах экстракции, фракционирования и импрегнации органических и неорганических веществ. Он является также перспективным рабочим телом для современных тепловых машин.
Техника безопасности По степени воздействия на организм человека газообразный диоксид углерода относится к 4-му классу опасности по ГОСТу 12.1.007-76 «Вредные вещества. Классификация и общие требования безопасности». Предельно допустимая концентрация в воздухе рабочей зоны не установлена, при оценке этой концентрации следует ориентироваться на нормативы для угольных и озокеритовых шахт, установленные в пределах 0,5%. При применении сухого льда, при использовании сосудов с жидкой низкотемпературной углекислотой должно обеспечиваться соблюдение мер безопасности, предупреждающих обморожение рук и других участков тела работника. |
gidro.tech-group.pro
Химические и физические свойства углекислого газа.
Углекислый газ (двуокись углерода), называемый также углекислотой, – важнейший компонент в составе газированных напитков. Он обусловливает вкус и биологическую стойкость напитков, сообщает им игристость и освежающие свойства.
Химические свойства. В химическом отношении углекислый газ инертен. Образовавшись с выделением большого количества тепла, он, как продукт полного окисления углерода, весьма стоек. Реакции восстановления двуокиси углерода протекают только при высоких температурах. Так, например, взаимодействуя с калием при 230° С, углекислый газ восстанавливается до щавелевой кислоты:
Вступая в химическое взаимодействие с водой, газ, в количестве не более 1% от содержания его в растворе, образует угольную кислоту, диссоциирующую на ионы Н+, НСО3–, СО23-. В водном растворе углекислый газ легко вступает в химические реакции, образуя различные углекислые соли. Поэтому водный раствор углекислого газа обладает большой агрессивностью по отношению к металлам, а также разрушающе действует на бетон.
Физические свойства. Для сатурации напитков используется углекислый газ, приведенный в жидкое состояние сжатием до высокого давления. В зависимости от температуры и давления углекислый газ может находиться также в газообразном и твердом состоянии. Температура и давление, соответствующие данному агрегатному состоянию, приведены на диаграмме фазового равновесия (рис. 13).
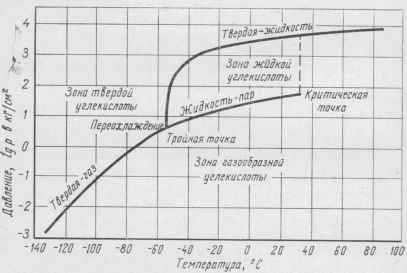
Рис. 13. Диаграмма фазового равновесия углекислого газа.
При температуре минус 56,6° С и давлении 0,52 Мн/м2 (5,28 кГ/см2), соответствующих тройной точке, углекислый газ может одновременно находиться в газообразном, жидком и твердом состоянии. При более высоких температуре и давлении углекислый газ находится в жидком и газообразном состоянии; при температуре и давлении, которые ниже этих показателей, газ, непосредственно минуя жидкую фазу, переходит в газообразное состояние (сублимирует). При температуре, превышающей критическую температуру 31,5° С, никакое давление не может удержать углекислый газ в виде жидкости.
В газообразном состоянии углекислый газ бесцветен, не имеет запаха и обладает слабовыраженным кислым вкусом. При температуре 0° С и атмосферном давлении плотность углекислого газа составляет 1,9769 кг/ж3; он в 1,529 раз тяжелее воздуха. При 0°С и атмосферном давлении 1 кг газа занимает объем 506 л. Связь между объемом, температурой и давлением углекислого газа выражается уравнением:
где V – объем 1 кг газа в м3/кг; Т – температура газа в ° К; Р – давление газа в н/м2; R – газовая постоянная; А – дополнительная величина, учитывающая отклонение от уравнения состояния идеального газа;
Ожиженный углекислый газ – бесцветная, прозрачная, легкоподвижная жидкость, напоминающая по внешнему виду спирт или эфир. Плотность жидкости при 0° С равна 0,947. При температуре 20°С ожиженный газ сохраняется под давлением 6,37 Мн/м2 (65 кГ/см2) в стальных баллонах. При свободном истечении из баллона жидкость испаряется с поглощением большого количества тепла. При снижении температуры до минус 78,5° С часть жидкости замерзает, превращаясь в так называемый сухой лед. По твердости сухой лед близок к мелу и имеет матово-белый цвет. Сухой лед испаряется медленнее жидкости, при этом он непосредственно переходит в газообразное состояние.
При температуре минус 78,9° С и давлении 1 кГ/см2 (9,8 Мн/м2) теплота сублимации сухого льда составляет 136,89 ккал/кг (573,57 кдж/кг).
www.comodity.ru
Физические и химические свойства углекислого газа: формула,плотность
Применение углекислого газа в сварочной области является очень распространенной. Это один из основных вариантов, которые применяются для различных видов соединения металла. Физические свойства углекислого газа определяют его как универсальную субстанцию для газовой сварки, соединения газовой и электродуговой и так далее. Это относительно недорогое сырье, которое используется здесь на протяжении многих лет. Есть более эффективные варианты, но именно углекислота применяется чаще всего. Она находит применение как для обучения, так и для выполнения самых простых процедур.
Углекислота еще носит название диоксид углерода. Вещество не обладает запахом и бесцветно в обыкновенном состоянии. При нормальном атмосферном давлении, углекислота не состоит в жидком состоянии и из твердого сразу переходит в газообразное.
Область применения углекислого газа
Химическое вещество используется не только для сварки. Физические свойства углекислого газа позволяют применять его как разрыхлитель или консервант в пищевой промышленности. Во многих системах пожаротушения, в частности в ручных огнетушителях. Его применяют для обеспечения питания аквариумных растений. Практически все газированные напитки содержат углекислый газ.
В сварочной сфере применение чистой углекислоты является не совсем безопасным для металла. Дело в том, что при воздействии высокой температуры он распадается и из него выделяется кислород. В свою очередь, кислород является опасным для сварочной ванны и чтобы ликвидировать его негативное воздействие, применяют разнообразные раскислители, такие как кремний и марганец.
Применение углекислоты встречается еще и в баллонах для пневматических пистолетов и винтовок. Как и в сварочных баллонах, углекислота здесь хранится в сжиженном состоянии под давлением.

Баллон с углекислотой для сварки
Химическая формула
Химические свойства углекислого газа, а также его другие характеристики, напрямую зависят от элементов, которые входят в состав формулы. Формула углекислого газа в химии имеет вид CO2. Это означает, что углекислота содержит в себе один атом углерода и два атома кислорода.
Химические и физические свойства
Рассмотрев, как обозначается химических газ в химии, стоит более внимательно рассмотреть его свойства. Физические свойства углекислого газа проявляются в различных параметрах. Плотность углекислого газа при стандартных атмосферных условиях составляет 1,98 кг/м3. Это делает его в 1,5 раза тяжелее, чем воздух в атмосфере. Диоксид углерода не имеет запаха и цвета. Если его подвергнуть сильному охлаждению, то он начинает кристаллизоваться в так называемый «сухой лед». Температура сублимации достигает -78 градусов Цельсия.
Химические свойства углекислого газа определяют его к кислотным оксидам, так как он может образовывать угольную кислоту, когда его растворяют в воде. При взаимодействии с щелочами, вещество начинает образовывать гидрокарбонаты и карбонаты. С некоторыми веществами, такими как фенол, диоксид углерода вступает в реакцию электрофильного замещения. С магнийорганическими вещество вступает в реакцию нуклеофильного присоединения. Использование углекислоты в огнетушителях обусловлено тем, что она не поддерживает процесс горения. Использование в сварке обусловлено тем, что в веществе горят некоторые активные металлы.
Преимущества
- Использование углекислого газа является относительно недорогим, так как цена на данное вещество достаточно низкая, если сравнивать с другими газами;
- Это очень распространенное вещество, найти которое можно во многих местах;
- Углекислый газ удобен в хранении и не требует сверхсложных мер безопасности;
- Газ хорошо справляется с теми обязанностями, для которых он предназначается.
Недостатки
- Во время использования на металле могут образовываться оксиды, которые выделяет вещество во время нагревания;
- Для нормальной работы нужно использовать дополнительные расходные материалы, которые бы помогли ликвидировать негативное воздействие оксидов;
- Существуют более эффективные газы, применяемые в сварочной сфере.
Применение углекислого газа при сварке
Данное вещество применяется в области сваривания металлических изделий в качестве защитного газа. Он применяется как для автоматических, так и для полуавтоматических сварочных аппаратов. Зачастую его используют не в чистом виде а вместе с аргоном или кислородом в газовой смеси. В производственной сфере существует несколько вариантов снабжения постов. Среди них выделяют следующие методы:
- Поставка из баллона. Это очень удобно, когда речь идет об относительно небольших объемах вещества. Это обеспечивает мобильность, так как не всегда имеется возможность создать трубопровод к посту.
- Транспортная емкость для углекислоты. Это также отличный вариант для потребления вещества в небольших баллонах. Она обеспечивает поставку большего количества газа, чем в баллонах, но менее удобна в транспортировке.
- Стационарный сосуд накопитель. Он применяется для тех, кто использует углекислоту в больших объемах. Их используют при отсутствии на предприятии автономной станции.
- Автономная станция. Это наиболее широкий по объему метод поставки, так как может обслуживать пост практически для любых процедур, вне зависимости от объемов. Таким образом, пост получает вещество непосредственно с места его производства.
Автономная станция представляет собой специальный цех на предприятии, где получают диоксид углерода. Он может работать как исключительно для собственных нужд, так и на поставку другим цехам и организациям. Для обеспечения рабочих точек предприятия, газ поставляет по трубопроводам. В то время, когда на предприятии имеется необходимость в запасании углекислоты, ее перемещают в специальные накопители.
Меры безопасности
Хранение и использование вещества является относительно безопасным. Но для того, чтобы исключить вероятности несчастных случаев, следует придерживаться основных правил:
- Несмотря на то, что углекислота не отличается взрывоопасностью и токсичностью, если ее концентрация будет выше 5%, то человек будет чувствовать удушье и кислородную недостаточность. Не следует допускать утечки и хранения всего в закрытом не проветриваемом помещении.
- Если понизить давление, то жидкая углекислота превращается в газообразное состояние. В это время ее температура может составлять -78 градусов Цельсия. Это вредно для слизистых оболочек организма. Также это приводит к обморожению кожи
- Осмотр больших емкостей для хранения углекислоты следует проводить с использованием шлангового противогаза. Цистерна должна быть отогрета до температуры окружающей среды и быть хорошо проветренной.
Заключение
Физические свойства являются не единственным показателем, по которому подбирается газ для сварки. Совокупность всех параметров обеспечивает данному веществу уверенные позиции на современном рынке расходных материалов. Среди самых простых процедур это незаменимый газ, с которым сталкивался практически каждый профессиональный и начинающий сварщик.
svarkaipayka.ru
Основные химические свойства углекислого газа
Прежде чем рассматривать химические свойства углекислого газа, выясним некоторые характеристики данного соединения.
Общие сведения
Углекислый газ является важнейшим компонентом газированной воды. Именно он придает напиткам свежесть, игристость. Данное соединение является кислотным, солеобразующим оксидом. Относительная молекулярная масса углекислого газа составляет 44 г/моль. Этот газ тяжелее воздуха, поэтому скапливается в нижней части помещения. Данное соединение плохо растворяется в воде.

Химические свойства
Рассмотрим химические свойства углекислого газа кратко. При взаимодействии с водой происходит образование слабой угольной кислоты. Она практически сразу после образования диссоциирует на катионы водорода и анионы карбоната или гидрокарбоната. Полученное соединение вступает во взаимодействие с активными металлами, оксидами, а также со щелочами.
Каковы основные химические свойства углекислого газа? Уравнения реакций подтверждают кислотный характер данного соединения. Оксид углерода (4) способен образовывать карбонаты с основными оксидами.
Физические свойства
При нормальных условиях данное соединение находится в газообразном состоянии. При повышении давления можно перевести его до жидкого состояния. Этот газ не имеет цвета, лишен запаха, обладает незначительным кислым вкусом. Сжиженная углекислота является бесцветной, прозрачной, легкоподвижной кислотой, аналогичной по своим внешним параметрам эфиру либо спирту.
Относительная молекулярная масса углекислого газа составляет 44 г/моль. Это практически в 1,5 раза больше, чем у воздуха.
В случае понижения температуры до -78,5 градусов по Цельсию происходит образование сухого льда. Он по своей твердости аналогичен мелу. При испарении данного вещества образуется газообразный оксид углерода (4).
Качественная реакция
Рассматривая химические свойства углекислого газа, необходимо выделить его качественную реакцию. При взаимодействии данного химического вещества с известковой водой (гидроксидом кальция) происходит образование мутного осадка карбоната кальция.
Кавендишу удалось обнаружить такие характерные физические свойства оксида углерода (4), как растворимость в воде, а также высокий удельный вес.
Лавуазье был проведен химический эксперимент, в ходе которого он пытался из оксида винца выделить чистый металл.
Выявленные в результате подобных исследований химические свойства углекислого газа стали подтверждением восстановительных свойств данного соединения. Лавуазье при прокаливании окиси свинца с оксидом углерода (4) сумел получить металл. Для того чтобы удостовериться в том, что второе вещество является оксидом углерода (4), он пропустил через газ известковую воду.
Все химические свойства углекислого газа подтверждают кислотный характер данного соединения. В земной атмосфере данное соединение содержится в достаточном количестве. При систематическом росте в земной атмосфере данного соединения возможно серьезное изменение климата (глобальное потепление).
Именно диоксид углерода играет важную роль в живой природе, ведь данное химическое вещество принимает активное участие в метаболизме живых клеток. Именно это химическое соединение является результатом разнообразных окислительных процессов, связанных с дыханием живых организмов.
Углекислый газ, содержащийся в земной атмосфере, является основным источником углерода для живых растений. В процессе фотосинтеза (на свету) происходит процесс фотосинтеза, который сопровождается образованием глюкозы, выделением в атмосферу кислорода.
Диоксид углерода не обладает токсичными свойствами, он не поддерживает дыхания. При повышенной концентрации данного вещества в атмосфере у человека возникает задержка дыхания, появляются сильные головные боли. В живых организмах углекислый газ имеет важное физиологическое значение, к примеру, он необходим для регуляции сосудистого тонуса.
Особенности получения
В промышленных масштабах углекислоту можно выделять из дымового газа. Кроме того, СО2 является побочным продуктом разложения доломита, известняка. Современные установки для производства углекислого газа предполагают использование водного раствора этанамина, адсорбирующего газ, содержащийся в дымовом газе.
В лаборатории диоксид углерода выделяют при взаимодействии карбонатов или гидрокарбонатов с кислотами.

Применение углекислого газа
Данный кислотный оксид применяется в промышленности в качестве разрыхлителя или консерванта. На упаковке продукции данное соединение указывается в виде Е290. В жидком виде углекислоту используют в огнетушителях для тушения пожаров. Оксид углерода (4) используют для получения газированной воды и лимонадных напитков.
fb.ru
Плотность углекислого газа (CO2), значение и примеры
Плотность углекислого газа и другие его физические свойства
Он плохо растворяется в воде, частично реагируя с ней.
Основные константы углекислого газа приведены в таблице ниже.
Таблица 1. Физические свойства и плотность углекислого газа.
|
Плотность, кг/м3 |
1,9768 |
|
Удельная теплота плавления, кДж/моль |
25,13 |
|
Динамическая вязкость, Па×с |
8,5×10-5 |
|
Молярная масса, г/моль |
44,01 |
Углекислый газ играет важную роль в биологических (фотосинтез), природных (парниковый эффект) и геохимических (растворение в океанах и образование карбонатов) процессах. В больших количествах он поступает в окружающую среду в результате сжигания органического топлива, гниения отходов и др.
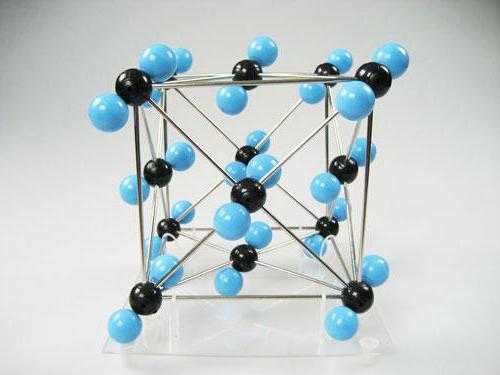
Химический состав и строение молекулы углекислого газа
Химический состав молекулы углекислого газа выражается эмпирической формулой CO2. Молекула диоксида углерода (рис. 1) линейная, что соответствует минимальному отталкиванию связывающих электронных пар, длина связи С=Щ равна 0,116 нм, а её средняя энергия – 806 кДж/моль. В рамках метода валентных связей две σ-связи С-О образованы sp-гибридизованнойорбиталью атома углерода и 2pz – орбиталями атомов кислорода. Не участвующие в sp-гибридизации 2px— и 2py-орбитали атома углерода перекрываются с аналогичными орбиталями атомов кислорода. При этом образуются две π-орбитали, расположенные во взаимно перпендикулярных плоскостях.
Рис. 1. Строение молекулы углекислого газа.
Благодаря симметричному расположению атомов кислорода молекула CO2 неполярная, поэтому диоксид мало растворим в воде (один объем CO2 в одном объеме H2O при 1 атм и 15oС). Неполярность молекулы приводит к слабым межмолекулярным взаимодействия и низкой температуре тройной точки: t = -57,2oС и P = 5,2 атм.
Краткое описание химических свойств и плотность углекислого газа
Химически углекислый газ инертен, что обусловлено высокой энергией связей O=C=O. С сильными восстановителями при высоких температурах диоксид углерода проявляет окислительные свойства. Углем он восстанавливается до угарного газа CO:
C + CO2 = 2CO (t = 1000oC).
Магний, зажженный на воздухе, продолжает гореть и в атмосфре углекислого газа:
CO2 + 2Mg = 2MgO + C.
Оксид углерода (IV) частично реагирует с водой:
CO2(l) + H2O = CO2×H2O(l) ↔ H2CO3(l).
Проявляет кислотные свойства:
CO2 + NaOHdilute = NaHCO2;
CO2 + 2NaOHconc = Na2CO3 + H2O;
CO2 + Ba(OH)2 = BaCO3↓ + H2O;
CO2 + BaCO3(s) + H2O = Ba(HCO3)2(l).
При нагревании до температуры свыше 2000oС углекислый раз разлагается:
2CO2 = 2CO + O2.
Примеры решения задач
ru.solverbook.com
свойства, получение, применение :: SYL.ru
Вы уже знаете, что при выдохе из легких выходит углекислый газ. А вот что вам известно об этом веществе? Наверное, немного. Сегодня я отвечу на все вопросы, касающиеся углекислого газа.
Определение
Это вещество в нормальных условиях является бесцветным газом. Во многих источниках его могут называть по-разному: и оксидом углерода (IV), и угольным ангидридом, и двуокисью углерода, и диоксидом углерода.
Свойства
Углекислый газ (формула СО2) является бесцветным газом, имеющим кислые запах и вкус, растворимым в воде веществом. Если его как следует охладить, то образуется снегообразная масса, называемая сухим льдом (фотография ниже), которая сублимирует при температуре -78оС.  Является одним из продуктов гниения или горения любого органического вещества. Растворяется в воде только при температуре 15оС и только в том случае, если отношение вода:углекислый газ равно 1:1. Плотность углекислого газа может быть разной, но в стандартных условиях она равняется 1,976 кг/м3. Это если он находится в газообразном виде, а в других состояниях (жидком/газообразном) значения плотности тоже будут другими. Данное вещество является кислотным оксидом, его добавление в воду приводит к получению угольной кислоты. Если соединить углекислый газ с любой щелочью, то в результате последующей реакции образуются карбонаты и гидрокарбонаты. Этот оксид не может поддерживать горение, кроме некоторых исключений. Это активные металлы, и при реакции такого вида они забирают у него кислород.
Является одним из продуктов гниения или горения любого органического вещества. Растворяется в воде только при температуре 15оС и только в том случае, если отношение вода:углекислый газ равно 1:1. Плотность углекислого газа может быть разной, но в стандартных условиях она равняется 1,976 кг/м3. Это если он находится в газообразном виде, а в других состояниях (жидком/газообразном) значения плотности тоже будут другими. Данное вещество является кислотным оксидом, его добавление в воду приводит к получению угольной кислоты. Если соединить углекислый газ с любой щелочью, то в результате последующей реакции образуются карбонаты и гидрокарбонаты. Этот оксид не может поддерживать горение, кроме некоторых исключений. Это активные металлы, и при реакции такого вида они забирают у него кислород.
Получение
Углекислый и еще некоторые газы в больших количествах выделяются, когда производят алкоголь или разлагаются природные карбонаты. Затем полученные газы проходят промывание растворенным карбонатом калия. Далее следует поглощение ими углекислого газа, продуктом данной реакции является гидрокарбонат, при нагревании раствора которого получают искомый оксид. Но сейчас его с успехом заменяет растворенный водой этаноламин, который абсорбирует содержащийся в дымовом газе оксид углерода и отдает его при нагревании. Также этот газ является побочным продуктом тех реакций, при которых получают чистые азот, кислород и аргон. В лаборатории немного углекислоты получается, когда карбонаты и гидрокарбонаты взаимодействуют с кислотами. Еще она образуется, когда реагируют пищевая сода и лимонный сок или тот же гидрокарбонат натрия и уксус (фото).
Применение
Пищевая промышленность не может обойтись без использования углекислоты, где она известна в качестве консерванта и разрыхлителя, имеющего код E290. Ее в виде жидкости содержит любой огнетушитель.  Также оксид четырехвалентного углерода, который выделяется в процессе брожения, служит хорошей подкормкой аквариумным растениям. Он содержится и во всем известной газировке, которую многие довольно часто покупают в продуктовом магазине. Сварка проволокой происходит в углекислой среде, но если температура данного процесса очень высока, то он сопровождается диссоциацией углекислоты, при которой выделяется кислород, окисляющий металл. Тогда сварка не обходится без раскислителей (марганца или кремния). Углекислым газом накачивают велосипедные колеса, он присутствует и в баллончиках пневматического оружия (такая его разновидность называется газобаллонной). Также данный оксид в твердом состоянии, называемый сухим льдом, нужен как хладагент в торговле, научных исследованиях и при починке некоторой техники.
Также оксид четырехвалентного углерода, который выделяется в процессе брожения, служит хорошей подкормкой аквариумным растениям. Он содержится и во всем известной газировке, которую многие довольно часто покупают в продуктовом магазине. Сварка проволокой происходит в углекислой среде, но если температура данного процесса очень высока, то он сопровождается диссоциацией углекислоты, при которой выделяется кислород, окисляющий металл. Тогда сварка не обходится без раскислителей (марганца или кремния). Углекислым газом накачивают велосипедные колеса, он присутствует и в баллончиках пневматического оружия (такая его разновидность называется газобаллонной). Также данный оксид в твердом состоянии, называемый сухим льдом, нужен как хладагент в торговле, научных исследованиях и при починке некоторой техники.
 Заключение
Заключение
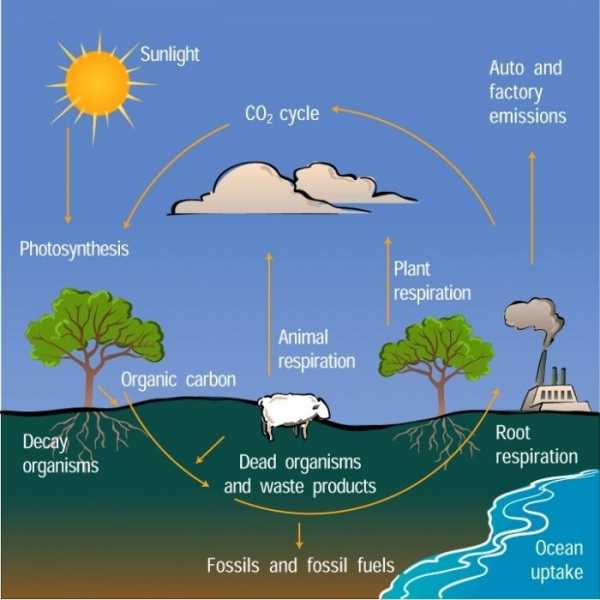
Вот до чего полезен для человека углекислый газ. И не только в промышленности, он играет и важную биологическую роль: без него не может происходить газообмен, регуляция сосудистого тонуса, фотосинтез и многие другие природные процессы. Но его переизбыток или недостача в воздухе некоторое время могут негативно влиять на физическое состояние всех живых организмов.
www.syl.ru
объем, масса и сгорание углекислого газа
Углекислый газ, или диоксид углерода, или CO2 — одно из самых распространенных на Земле газообразных веществ. Он окружает нас в течение всей нашей жизни. Углекислый газ не имеет цвета, вкуса и запаха и никак не ощущается человеком.
 Углекислый газ
Углекислый газОн является важным участником обмена веществ живых организмов. Газ сам по себе не ядовит, но не поддерживает дыхание, поэтому превышение его концентрации ведет к ухудшению снабжения тканей организма кислородом и к удушью. Углекислый газ широко применяется в быту и в промышленности.
Что такое диоксид углерода
При атмосферном давлении и комнатной температуре диоксид углерода находится в газообразном состоянии. Это наиболее часто встречающаяся его форма, в ней он участвует в процессах дыхания, фотосинтеза и обмена веществ живых организмов.

Диоксид углерода
При охлаждении до -78 °С он, минуя жидкую фазу, кристаллизуется и образует так называемый «сухой лед», широко применяемый как безопасный хладагент в пищевой и химической промышленности и в уличной торговле и рефрижераторных перевозках.
При особых условиях — давлении в десятки атмосфер — углекислота переходит в жидкое агрегатное состояние. Это происходит на морском дне, на глубине свыше 600 м.
Свойства углекислого газа
В 17 веке Жан-Батист Ван Гельмонт из Фландрии открыл углекислый газ и определил его формулу. Подробное исследование и описание было сделано столетие спустя шотландцем Джозефом Блэком. Он исследовал свойства углекислого газа и провел серию опытов, в которых доказал, что он выделяется при дыхании животных.
В состав молекулы вещества входит один атом углерода и два атома кислорода. Химическая формула углекислого газа записывается как CO2
В нормальных условиях не обладает вкусом, цветом и запахом. Только вдыхая большое его количество, человек ощущает кислый привкус. Его дает угольная кислота, образующаяся в малых дозах при растворении углекислого газа в слюне. Эта особенность применяется для приготовления газированных напитков. Пузырьки в шампанском, просекко, пиве и лимонаде — это и есть углекислый газ, образовавшийся в результате естественных процессов брожения или добавленный в напиток искусственно.

Физические свойства углекислого газа
Плотность углекислого газа больше плотности воздуха, поэтому при отсутствии вентиляции он скапливается внизу. Он не поддерживает окислительные процессы, такие, как дыхание и горение.
Поэтому углекислоту применяют в огнетушителях. Это свойство углекислого газа иллюстрируют с помощью фокуса — горящую свечу опускают в «пустой» стакан, где она и гаснет. В действительности стакан заполнен CO2.
Углекислый газ в природе естественные источники
К таким источникам относятся окислительные процессы разной интенсивности:
- Дыхание живых организмов. Из школьного курса химии и ботаники все помнят, что в ходе фотосинтеза растения поглощают углекислый газ и выделяют кислород. Но не все помнят, что это происходит только днем, при достаточном уровне освещения. В темное время суток растения наоборот, поглощают кислород и выделяют углекислый газ. Так что попытка улучшить качество воздуха в комнате, превращая ее в заросли фикусов и герани может сыграть злую шутку.
- Извержения и другая вулканическая активность. CO2 выбрасывается из глубин мантии Земли вместе с вулканическими газами. В долинах рядом с источниками извержений газа настолько много, что, скапливаясь в низинах, он вызывает удушье животных и даже людей. Известны несколько случаев в Африке, когда задыхались целые деревни.
- Горение и гниение органики. Горение и гниение — это одна и та же реакция окисления, но протекающая с разной скоростью. Богатые углеродом разлагающиеся органические остатки растений и животных, лесные пожары и тлеющие торфяники — все это источники диоксида углерода.
- Самым же большим природным хранилищем CO2 являются воды мирового океана, в которых он растворен.
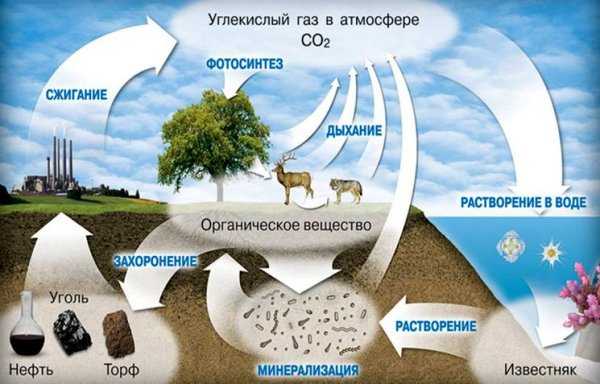
Углекислый газ в природе
За миллионы лет эволюции основанной на углеродных соединениях жизни на Земле в различных источниках накопились многие миллиарды тонн углекислого газа. Его одномоментный выброс в атмосферу приведет к гибели всего живого на планете из-за невозможности дыхания. Хорошо, что вероятность такого одномоментного выброса стремится к нулю.
Искусственные источники углекислого газа
Углекислый газ попадает в атмосферу и в результате человеческой жизнедеятельности. Самыми активными источниками в наше время считаются:
- Индустриальные выбросы, происходящие в ходе сгорания топлива на электростанциях и в технологических установках
- Выхлопные газы двигателей внутреннего сгорания транспортных средств: автомобилей, поездов, самолетов и судов.
- Сельскохозяйственные отходы — гниение навоза в больших животноводческих комплексах
Кроме прямых выбросов, существует и косвенное воздействие человека на содержание CO2 в атмосфере. Это массовая вырубка лесов в тропической и субтропической зоне, прежде всего в бассейне Амазонки.
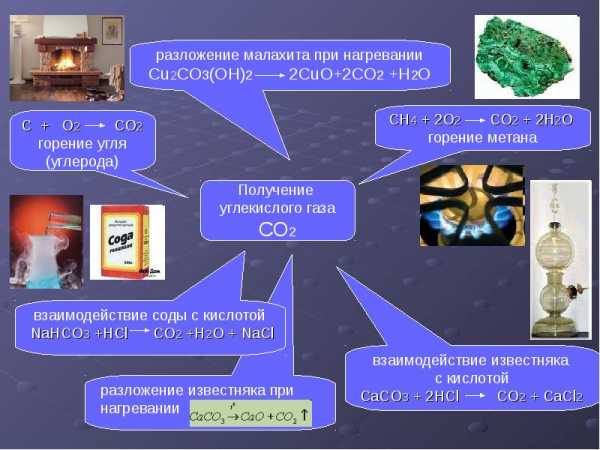
Искусственный источник углекислого газа
Несмотря на то, что в атмосфере Земли содержится менее процента диоксида углерода, он оказывает все возрастающее действие на климат и природные явления. Углекислый газ участвует в создании так называемого парникового эффекта путем поглощения теплового излучения планеты и удерживания этого тепла в атмосфере. Это ведет к постепенному, но весьма угрожающему повышению среднегодовой температуры планеты, таянию горных ледников и полярных ледяных шапок, росту уровня мирового океана, затоплению прибрежных регионов и ухудшению климата в далеких от моря странах.
Знаменательно, что на фоне общего потепления на планете происходит значительное перераспределение воздушных масс и морских течений, и в отдельных регионах среднегодовая температура не повышается, а понижается. Это дает козыри в руки критикам теории глобального потепления, обвиняющим ее сторонников в подтасовке фактов и манипуляции общественным мнением в угоду определенным политическим центрам влияния и финансово-экономическим интересам
Человечество пытается взять под контроль содержание углекислого газа в воздухе, были подписаны Киотский и Парижский протоколы, накладывающие на национальные экономики определенные обязательства. Кроме того, многие ведущие автопроизводители автомобилей объявили о сворачивании к 2020-25 годам выпуска моделей с двигателями внутреннего сгорания и переходе на гибриды и электромобили. Однако некоторые ведущие экономики мира, такие, как Китай и США, не торопятся выполнять старые и брать на себя новые обязательства, мотивируя это угрозой уровню жизни в своих странах.
Углекислый газ и мы: чем опасен CO2
Углекислый газ — один из продуктов обмена веществ в организме человека. Он играет большую роль в управлении дыханием и снабжением кровью органов. Рост содержания CO2 в крови вызывает расширение сосудов, способных таким образом транспортировать больше кислорода к тканям и органам. Аналогично и система дыхания понуждается к большей активности, если концентрация углекислоты в организме растет. Это свойство используют в аппаратах искусственной вентиляции легких, чтобы подстегнуть собственные органы дыхания пациента к большей активности.
Кроме упомянутой пользы, превышение концентрации СO2 может принести организму и вред. Повышенное содержание во вдыхаемом воздухе приводит к тошноте, головной боли, удушью и даже к потере сознания. Организм протестует против углекислого газа и подает человеку сигналы. При дальнейшем увеличении концентрации развивается кислородное голодание, или гипоксия. Co2 мешает кислороду присоединяться к молекулам гемоглобина, которые и осуществляют перемещение связанных газов по кровеносной системе. Кислородное голодание ведет к снижению работоспособности, ослаблению реакции и способностей к анализу ситуации и принятию решений, апатии и может привести к смерти.
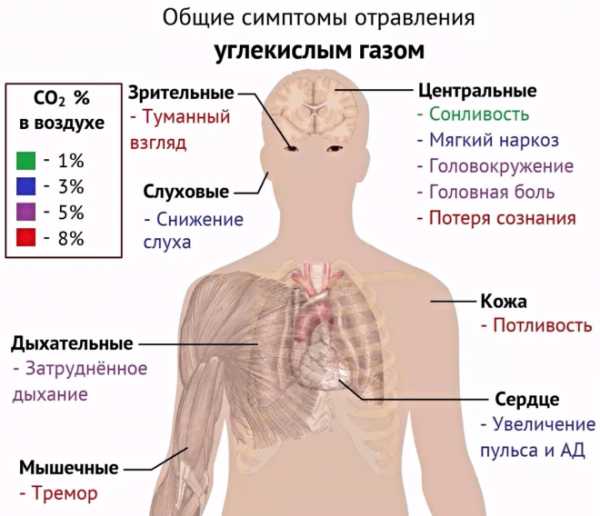
Общие симптомы отравления углекислым газом
Такие концентрации углекислого газа, к сожалению, достижимы не только в тесных шахтах, но и в плохо проветриваемых школьных классах, концертных залах, офисных помещениях и транспортных средствах — везде, где в замкнутом пространстве без достаточного воздухообмена с окружающей средой скапливается большое количество людей.
Основное применение
CO2 широко применяется в промышленности и в быту – в огнетушителях и для изготовления газировки, для охлаждения продуктов и для создания инертной среды при сварке.

Основное применение углекислого газа
Применение углекислого газа отмечено в таких отраслях, как:
- для чистки поверхностей сухим льдом.
Фармацевтика
- для химического синтеза компонентов лекарственных средств;
- создания инертной атмосферы;
- нормализация индекса pH отходов производства.

Углекислый газ в фармацевтике
Пищевая отрасль
- производство газированных напитков;
- упаковка продуктов питания в инертной атмосфере для продления срока годности;
- декаффеинизация кофейных зерен;
- замораживание или охлаждение продуктов.

Углекислый газ в пищевой отрасли
Медицина, анализы и экология
- Создание защитной атмосферы при полостных операциях.
- Включение в дыхательные смеси в качестве стимулятора дыхания.
- В хроматографических анализах.
- Поддержание уровня pH в жидких отходах производства.

Углекислый газ и экология
Электроника
- Охлаждение электронных компонентов и устройств при тестировании на температурную стойкость.
- Абразивная очистка в микроэлектронике (в твердой фазе).
- Очищающее средство в производстве кремниевых кристаллов.
Химическая отрасль
Широко применяется в химическом синтезе в качестве реагента и в качестве регулятора температур в реакторе. CO2 отлично подходит для обеззараживания жидких отходов с низким индексом pH.

Использование углекислого газа
Применяется также для осушения полимерных веществ, растительных или животных фиброматериалов, в целлюлозном производстве для нормализации уровня pH как компонентов основного процесса, так и его отходов.
Металлургическая отрасль
В металлургии CO2 в основном служит делу экологии, защиты природы от вредных выбросов путем их нейтрализации:

Применение углекислого газа в металлургии
- В черной металлургии — для нейтрализации плавильных газов и для донного перемешивания расплава.
- В цветной металлургии при производстве свинца, меди, никеля и цинка — для нейтрализации газов при транспортировке ковша с расплавом или горячих слитков.
- В качестве восстановительного агента при организации оборота кислотных шахтных вод.
Сварка в углекислой среде

Процесс сварки с применением углекислого газа
Разновидность сварки под флюсом является сварка в углекислой среде. Операции сварочных работ с углекислым газом осуществляется плавящимся электродом и распространен в процессе монтажных работ, устранении дефектов и исправления деталей с тонкими стенками.
Если вы нашли ошибку, пожалуйста, выделите фрагмент текста и нажмите Ctrl+Enter.
Вам также могут быть интересны статьи:
stankiexpert.ru

